医用导管是无菌导管,导尿管,鼻氧管,血管内导管等各种导管的总称,血液透析导管是紧急血液透析的血管通路,瘘管未成熟期或其他条件有限暂时不能做瘘管患者,也是长期透析患者的部分“生命线”。导管在人体内留置时间30天,产品应符合以下要求,并且通过导管测试仪检验达到以下标准后才可使用,主要的血管内导管测试仪器有GLL0285-D 血管内导管动力注射中流量与压力测试仪。
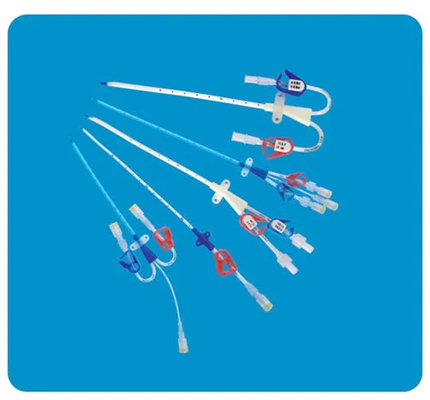
血管内导管测试标准:
YY 0285.1-2017《血管内导管一次性使用无菌导管 第1部分:通用要求》、
YY 0285.3-2017《血管内导管一次性使用无菌导管 第3部分:中心静脉导管》、
YY 0267-2016《血液透析及相关治疗血液净化装置的体外循环血路》;
辅助穿刺附件应符合YY 0450.1-2003《一次性使用无菌血管内导管附件第1部分:引导器械》、GB/T 18457-2015《制造医疗器械用不锈钢针管》等相关标准。
血管内导管生产
因此,在企业发展对于血透管的日常生活生产成本控制中,需要我们参考相关法律监管工作要求,结合产品市场风险,建立一个合适的风险监控点。结合公司产品具体工艺生产管理过程,对每一个过程和环节可以进行分析梳理,识别可能的风险,制定风险内部控制措施,开展控制措施的有效性验证,保障风险控制措施的有效性和在可接受水平范围内。
血管内导管测试现状
参见《医疗器械监督管理规定》、《医疗器械不良事件监测与再评价管理办法》、《医疗器械召回管理办法》、《医疗器械不良事件监测工作指南(试行)》。 查询国家药品不良反应监测中心网站,未发现血液透析导管不良事件。但是关于血管内导管测试企业自身要做好工作,无论是找检测机构还是自行购买血管内导管测试仪,都要符合测试标准才可将合格的医疗器械出售和使用。
血管内导管风险点分析
在采购中,材料本身的质量对半成品和成品的性能至关重要。不同材料对产品性能的影响不同,同一材料(物理、化学、微生物等)的不同性能对产品性能的影响也不同。
①供应商管理。建立供应商质量管理流程,建立物料质量标准,进行供应商评价和物料评估,确保生产质量稳定的合格供应商能够被列入合格供应商名单,减少因供应商供应能力而导致的物料异常,进而影响产品质量。
②对于某些高分子材料,在储存过程中可能会发生原料质量损失或失效。需要验证原材料的有效期,以确定原材料的可用时间。同样,对于一些可能受储存环境影响的物料(如温度、湿度、光线等。),需要确定物料最佳贮存环境的要求,防止贮存不当造成物料质量下降或失效,进而影响产品质量。
③原材料质量检验。建立信息质量检验和测试工作能力,包括系统测试技术设备、测试研究方法、测试管理人员等。建立原材料进货指导书,对材料工程质量问题进行相关检验,在流转到生产加工工序前,利用导管测试仪(GLL0285-D 血管内导管动力注射中流量与压力测试仪)识别材料可能影响存在的异常,将风险控制在前端。

GLL0285-D 血管内导管动力注射中流量与压力测试仪按照GB/T 15812.1-2005、YY 0285.1-2017标准设计制造,专门用于非血管内导管、血管内导管一次性使用无菌导管等医用导管类水流量的测定。

 联系QQ:16020642
联系QQ:16020642 联系邮箱:wangjing@weixia-china.com
联系邮箱:wangjing@weixia-china.com 传真:86-0571-88697266
传真:86-0571-88697266 联系地址:浙江省杭州市萧山区萧山经济技术开发区红垦农场红灿路189号联东U谷15幢
联系地址:浙江省杭州市萧山区萧山经济技术开发区红垦农场红灿路189号联东U谷15幢
扫一扫 微信咨询
©威夏电子科技(杭州)有限公司 版权所有 备案号:浙ICP备19049171号-10 GoogleSitemap 管理登陆